
��������
��һ�������������о�������4000-8000�֣���
1����Ŀ�������������о����塢�������о���״����չ��̬���������Ͽ�ѧ�о���չ������������ѧ���壻���Ϲ��ú���ᷢչ��������Ҫ����Ĺؼ��Ƽ�������������Ӧ��ǰ��������Ҫ�ο�����Ŀ¼����
��1�������
2006�������ձ�������ѧ��Shinya Yamanaka�ڡ�ϸ���������ȱ����˽�Oct3/4��Sox2��c-Myc��Klf4������ת¼��������С�������άϸ�������յ�ϸ���ر�̲����յ����ܸ�ϸ�� (induced pluripotent stem cell, iPS cell )�� ����������ϸ����ϸ����̬������͵��ױ�������Ŵ�����״̬��ϸ������������������ͻ�̥�������������ֻ������ȶ�涼����̥��ϸ������[1]�������о��ɹ������2012���ŵ��������
��̥��ϸ��֮��������㷺�Ĺ�ע����Ҫ����������ȫ���ԡ���Ϊһ������������̥������ϸ����������������������г������Ҹ��µ�����������Ҫ���DZ����˷ֻ�Ϊ���߲��DZ��[2]����̥��ϸ�������ȫ���������Ѿ��㷺�������Ƹ��༲�������������������Ӧ������Ϊ������ֲ�Ʒ����������Ʒ��Ŀǰ��������ֲ��ͻ����������Դ��ȱ����̥��ϸ����ȫ������ʾ���ǿɽ����յ��������ض������٣����������������١������ַ����м������Ե�ȱ�ݣ����ȣ�����������ֲ����̥��ϸ��������ģ���������������췴Ӧ�����һ�ȡ;��Ҳ���ޣ���Σ�һ�������ڼ������뵫��ȴ���ò����ǵ��������ڽ��������ɵȶ������ƣ���Ҳ����̥��ϸ���Ʒ�����ʵ�е�����ϰ�����ˣ�����ԴΪ�����еij���ϸ��������̥��ϸ����״���Ƶ�iPSϸ��һ�����֣����ܵ���ѧ�ҵĹ㷺��ע������ϣ�����ܽ����̥��ϸ����ҽ��Ӧ�������ٵļ������⡣
������ϸ���ر��ΪiPSϸ���������ض���֯���ٵĹ�����Ҫ�������������⣺һΪЧ�����⣬��Ϊ��ȫ��������������������յ��ر�̻�ȡiPSϸ���ijɹ����ʼ��ͣ�������ʱ�ϳ���֮���ѧ�Ҿ������ʵ�飬�ҵ�һЩ������Ӻʹ̼����ӣ������ض������µ�ijЩ�������ϸ���ܹ������ر��Ч�ʡ�����Щʵ��һ��ֻ�ܾ������ض���ϸ����ϵ���Һܶ��������ԣ�ʵ��Ŀ��ظ��Ȳ��ߣ�����ϸ���ر�̹����е�ϸ���ڲ��仯������δ��ȫ��ʶ�������ҵ����ʵ��ȶ���Ч��ȡiPSϸ���ķ�����������ʵ���У���Ҫʹ�ò�����Ϊ���壬����ʹ�õ��յ����ӱ���Ҳ�����°��ԡ��о������֣�����iPSϸ���ٴηֻ����γɻ�̥���ı���Ҳ�������ߡ���ȫ��������ʵ��iPSϸ���Ʒ����ģ�ٴ�Ӧ�����ٵ��ش����⣬�������һ����Ĺؼ�Ҳ�������˽�ϸ���ر�̻��Ƽ����漰�����ӡ�
����Ŀ�о����ں����е���Ը����ض���ϵ����ϸ�������ر�̵���ɢʵ�������Լ��ڶ��ϸ������ֻ�ʵ��ɹ����Աȳ���ϸ������̥��ϸ����iPSϸ���Լ����ڸ���ϵ�м�״̬��פ��ϸ�����ӻ��������ϸ������״̬̽����ͬ��ϵϸ���ر�̹��̵Ĺؼ��ڵ��Ӱ�����ӣ�����õ��ձ���ɽ�Ϊ��Ч��ȡ�ȶ���ȫ��iPSϸ���ṩ�������ݡ�
��2���������о���״
�ֽΣ�������ϸ���ر����Ҫʹ��ϸ���ںϼ���������ֲ�����Լ�ʹ��ϸ����ȡ������������ӽ����յ�����ȡiPSϸ�������У���ȡiPSϸ���ļ�����ȫ�����˶���̥��ϸ���������������ʵ����ϸ���ر�̵Ĺ��̡���������ת¼����OSKM �յ�ϸ���ر�̵��о��ɹ���һ�α�����֮�������о��Ŷӷ׳���ʹ�ò�ͬ�յ����ӶԲ�ͬ��ϵϸ�������ر�̡�
�����б����У�����άϸ����֬��ϸ����Ѫϸ����θ������ϸ������ϵ��ϸ�����гɹ�����ر�̵�ʵ��[3, 4]������ѧ��Ҳ���֣����ر�̵Ĺ����У�ijЩϸ�����ڶ���Դϸ���ļ���[5]���ڶ��ر�̵õ���iPSϸ�����зֻ��γɵڶ�����ϸ��ʱ�����Ǹ������ڷֻ�Ϊ��Դ��ϵ��ϸ��������ʾϸ���ر�̲�����ϸ���ֻ���һ����ȫ����̣�ijЩ�ο�����������˳������ת��������Щ��ʵ����ȴ�����ᷢ����ת��2014������ڿ�Cell�ϵ�һƪ�о������У��о���Vincent Pasqueͨ�������ر��ʱXȾɫ��ļ���������ڵ�ϸ��ˮƽ��ϸ����ת����̣���ϸ���ر��Ϊ��ϸ��������ν������¶���[6]�������ʾ����ϸ���ر�̹����з����ĸı����һ������ֽεķ�ʽ���������ý������в�ͬ���ر��ϵͳ�����в�ͬ��ϸ�������д��ڹ��ԡ��۲⼼���ķ�չʹ���ǿ���ȷ���κ�ϸ���ر�̵ľ�ȷ�Σ�����ǰ�ܶ��о��������˸�ϸ���ر�̵Ľ��ԣ������о����Խ��ر�̷�Ϊ�����Σ����ڣ�����ʼ���Σ����ںͺ��ڣ�������ȶ����Ρ���ʼ�εı�־�Ǽ�����Ƥת��ͨ·��MET��[7]����һ��ͨ������Ϊ������ģ����ڵ�ϸ��ˮƽ�µ��о�����������Ϊϸ���ر���г�����ȶ��ξ���ij�̶ֳȵ�ȷ��ʱ��[8]��
��ǰ���о�������ϸ���б����������͵����ԣ���ϸ���ر����ת�������Ե���̥�����ε�˳��������ϸ�����Ը�����ֻ���������ϵ�ľ�������ϵͳѰ�Ҳ�ͬ���ȶ�״̬�Ľ��[9]����ϵ�Կ�����ϸ���ر��Ҳ���ֽ�����Ϊ���ر�̽���������һС����ϸ���С�
ϸ���ر�̹�������ػ����һ�����鵰�����Ρ�DNA���������ֵ�Ⱦɫ��״̬�����ģʽת��Ϊ��һ��Ⱦɫ��״̬�����ģʽ������һ��������ز�β���ĸ��Ӷ�̬�������̡�һЩ�о�����Micro-array��Chip-chip��Chip-seq�ȶ���ʵ���ֶβ���iPSϸ������ͬ�λ�ͬ��̶̳ȵIJ����ر�̼�פ�����м�״̬ϸ���Ķ���ϵ�������鵰�����Ρ�DNA����״̬�ȣ����л���ر�̹����е������ӶԻ�����������ʱ��仯�Ĺ��ɣ���ʾ�ر��Ч�ʵ͵�ԭ��[10]�����о�������ϸ���ⲿ�����ź�ͨ·�������Ľ��ر��Ч�ʣ��ϵ���Nanog��Essrb������Ҳ�ɸĽ�Ч��[11]��2013�꣬Nature�Ϸ������о��ɹ����ֽ�2i/LIF����������OSKM���ȱ������ϣ��ټ���ʹMbd3/NuRD co-repressor�кͣ�������Ե�ȷ����ͬ�����ر�̾ͻ���֡���������7��ʱ���OSKM�յ�������100%��С���������ϸ����ת����˳�ʼ��iPSϸ��[12]�������о���Ҳ�Բ�ͬ״̬�����ϸ���������ϸ���ر��ʵ�飬�ҵ������ܹ�Ӱ���ر��Ч�ʵ��ź�ͨ·������[13-17]��2016�꣬����ѧ���ڿ�Nature�Ϸ�����һ�������о���չ��ʹ��һ�ֱ�����BRD3R�ļ�ø���嵰����Ϊ�ر�����ӣ��ɽ�Ƥ������άϸ���ر��Ϊ��iPSϸ����Ч��������20������ر��ʱ�����̼��죬ͬʱ����ر������[18]���ҹ���ѧ��������о�����,ά����C����ͨ�������Ŵ������������ iPSϸ�����յ�Ч��[19]��ϸ������������ϸ���ر��Ч�������й�ϵ��p53���ػ����о������˷�ϸ����ֹ����������ϸ����ֳ���ԸĽ��ر��Ч��,���ij�̶ֳ���֤ʵ�˸���������ϸ���ر��Ч���й���һ���ۣ���Ŀǰ�Դ�������ì�ܵĽ���[4]���������ϸ���ֻ����о���Ҳ�����ڶ������ϸ���ر�̻��Ƶ��о������ж����ض���ϵ�йؼ���������[20, 21]���ź�[22]��ʱ���ѡȡҲ����ҪӰ������[23, 24]��2016�꣬�����ڿ�Nature�Ϸ����������о�������е�������ϸ���������仯Ҳ���ϸ�����ر�̲���Ӱ��[25, 26]����֮��ϸ���ر����һ���漰�������ҷֽεĸ��ӹ��̣���������̵ľ����������ȷ�е��о����ۡ�
��3����Ҫ�ο���������
[1] K Takahashi, S Yamanaka. Induction of pluripotent stem cells from mouse embryonic and adult fibroblast cultures by defined factors[J]. Cell, 2006, 126: 663��676.
[2] MJ Evans, MH Kaufman. Establishment in culture of pluripotential cells from mouse embryos[J]. Nature, 1981, 292(5819): 154��156.
[3] N Maherali, R Sridharan, W Xie, et al. Directly reprogrammed fibroblasts show global epigenetic remodeling and widespread tissue contribution[J]. Cell Stem Cell, 2007, 1: 55��70.
[4] S Eminli, A Foudi, M Stadtfeld, et al. Differentiation stage determines potential of hematopoietic cells for reprogramming into induced pluripotent stem cells[J]. Nature Genetics, 2009, 41: 968��976.
[5] IB Dodd, MA Micheelsen, K Sneppen, et al. Theoretical analysis of epigenetic cell : memory by nucleosome modification[J]. Cell, 2007, 129: 813��822.
[6] V Pasque, J Tchieu, R Karnik, et al. X chromosome reactivation dynamics reveal stages of reprogramming to pluripotency[J]. Cell, 2014, 159(7): 1681��1697.
[7] RH Li, JL Liang, S Ni. A mesenchymal-to-epithelial transition initiates and is required for the nuclear reprogramming of mouse fibroblasts[J]. Cell Stem Cell, 2010, 7: 51��63.
[8] Y Buganim, DA Faddah, et al. Single-cell expression analyses during cellular reprogramming reveal an early stochastic and a late hierarchic phase[J]. 2012, 150: 1209��1222.
[9] V Chickarmane, C Peterson. A computational model for understanding stem cell, trophectoderm and endoderm lineage determination[J]. PLoS ONE, 2008, 3(10): e3478.
[10] TS Mikkelsen, J Hanna, X Zhang, et al. Dissecting direct reprogramming through integrative genomic analysis[J]. Nature, 2008, 454(7200): 49��55.
[11] J Hanna, K Saha, B Pando, et al. Direct cell reprogramming is a stochastic process amenable to acceleration[J]. Nature, 2009, 462(7273): 595��601.
[12] Y Rais, A Zviran,S Geula, et al. Deterministic direct reprogramming of somatic cells to pluripotency[J]. Nature, 2013, 502: 65��70.
[13] �¬B,������,�¼��,������. �յ��ر�̹����еı����Ŵ�����[J]. ���ﻯѧ������������չ,2015,11:1054��1062.
[14] J Shu, K Zhang, MJ Zhang, et al. GATA family members as inducers for cellular reprogramming to pluripotency[J]. Cell Research, 2015, 25: 169��180.
[15] XX Xu, Q Wang, Y Long, et al. Stress-mediated p38 activation promotes somatic cell reprogramming[J]. Cell Research,
[16] J Jiang, WJ Lv, XY Ye, et al. Zscan4 promotes genomic stability during reprogramming and dramatically improves the quality of iPS cells as demonstrated by tetraploid complementation[J]. Cell Research, 2013, 23: 92��106.
[17] GY Wang, XD Guo, WJ Hong, et al. Critical regulation of miR-200/ZEB2 pathway in Oct4/Sox2-induced mesenchymal-to-epithelial transition and induced pluripotent stem cell generation[J]. PNAS, 2013, 110(8): 2858��2863.
[18] ZC Shao, RW Zhang, A Khodadadi-Jamayran, et al. The acetyllysine reader BRD3R promotes human nuclear reprogramming and regulates mitosis[J]. Nature Communications, 2016, 7.
[19] ����,�½ݿ�,�����. ά����C������Ŵ���������[J]. ���ﻯѧ������������չ,2015,(11):1054��1062.
[20] PS Hoppe, M Schwarzfischer, D Loeffler, et al. Early myeloid lineage choice is not initiated by random PU.1 to GATA1 protein ratios[J]. Nature, 2016, 535: 299��302.
[21] T TeSlaa, AC Chaikovsky, I Lipchina, et al. ��-ketoglutarate accelerates the initial differentiation of primed human pluripotent stem cells[J]. Cell Metabolism, KM Loh, A Chen, PW Koh, et al. Mapping the pairwise choices leading from pluripotency to human bone, heart, and other mesoderm cell types[J]. Cell,
[22] IY Hwang, S Kwak, S Lee, et al. Psat1-dependent fluctuations in ��-ketoglutarate affect the timing of ESC differentiation[J]. Cell Metabolism, 2016, 24: 1��8.
[23] NA Ivanov, R Tao, JG Chenoweth, et al. Strong components of epigenetic memory in cultured human fibroblasts related to site of origin and donor age[J]. PLoS Genetics
[24] M Caiazzo, Y Okawa, A Ranga, et al. Defined three-dimensional microenvironments boost induction of pluripotency[J]. Nature Materials, 2016, 15: 344��352.
[25] HQ Le, S Ghatak, CYC Yeung, et al. Mechanical regulation of transcription controls Polycomb-mediated gene silencing during lineage commitment[J]. Nature Cell Biology,
2����Ŀ���о����ݡ��о�Ŀ�꣬�Լ������Ĺؼ���ѧ�������˲���Ϊ�ص�������ݣ���
��1�������
a. ȷ��ϸ���ر�̸��ιؼ�����ģ��
�����е�ϸ���ر��ʵ���������������ݣ��Ա���ϸ���������ر��ϸ����iPSϸ������̥��ϸ����ȷ�����������Բ�����������й��ܼ����ź�ͨ·������������ȷ����ϸ���ر�̸��γɹ����еĹؼ�����ģ�顣
b. ����ϸ���ر�̶�������ģ��
�ӻ���ת¼������������ijһ��ϵ��ϸ�����Ϳ�����ؼ������Ⱦɫ��״̬���������ģʽ��Ψһȷ�������ر�̹����У�ϸ�����Ϳ�����ϵ�����ԵĹؼ�����ı���ģʽ����������ϸ���ر�̶�������ģ���У�һ������ı���ģʽ���������ת¼���ϳɣ��ͽ����ʾ��������ȷ��ϸ���ر���л�������Ĺؼ�����ȷ��ת¼�ͽ����ʡ�ģ���а����ĸ���ҪӰ��ת¼�ͽ����ʵ����أ���1����ϵ�����Թؼ�������Ե��ںͻ����ڣ���2���ⲿ�źţ���3��Ⱦɫ�����λ�����Ŵ����ڵĿ���ЧӦ����4����ϸ�������ڻ�������ϵ����֮��Ͳ�ͬ��ϵ֮��ĶԿ���ϵ����ˣ��о���Ҫ������Щ���ض�ת¼�ͽ����ʵ�Ӱ�죬Ȼ�����Ǽ��ɵ����������ַ����С�
c. ģ��ϸ���ر�̷ֲ�仯����
�������о��з��ֵ��ر�̾��н�����Ϊ�����㣬���չؼ�����ļ������Ĭ״̬ͨ�������ļ��轨��ϸ���ر�̵����ηֲ�ģ�ͣ�ģ���ر�̹�����ϸ��������ص�����״̬��·����ÿһ��α仯��Ҫ�漰�ؼ�����ı��������״̬���ġ�
��2���о�Ŀ��
�������е�ϸ���ر��ʵ�����ݣ��Ƚ���ϸ���������ر��ϸ����iPSϸ������̥��ϸ���Ļ�����������״̬��ȷ�������������ݲ���������Ĺ��ܼ����ź�ͨ·������������ϵ�������������硢���ת¼���ӽ���������ȷϸ���ر�̹�������ϵ�ؼ�����ļ����Ĭ����Ҫ�¼������ر��Ч�ʵ�Ӱ�죻�������ð���ϸ������ת¼�����Ե����뻥���ء���ػ���Ⱦɫ�����ο���״̬����ϵϸ���ؼ�����֮��ĶԿ����ⲿ�źŷ���ͨ·��ϸ����ֳ���ڽṹ�ȶ��ε�����Ϣ��������ϸ��ˮƽ�ϵ�ϸ�����˿�����صĹؼ�����ĸ���ͳ�Ƶ���ģ�ͣ���ʵ������ѵ��ģ�Ͳ����Ӷ�����ϸ���ֲ����������
��3�������Ĺؼ����⣺
a. ȷ���ؼ�����ģ��Ĺؼ�����
ϸ���ر��ʱ������ϵѡ�����ϵ������������ϵ�Ĺؼ���������ص����ڽ���ϵ�ж���ؼ�������Ϊ����ģ�鿼��ʱ��Ҫ����������ԣ���ȡ��������ء�
b. ������������ģ�͵Ĺؼ�����
��θ��ݶ�Ӧ��ϵϸ��������ת¼���ӵ��Ե����뻥���ء��ⲿ�źŷ���ͨ·���鵰�����Ρ�DNA��������ϵ֮��ĶԿ��������ء�mRNA�������ء����ϳ��뽵��ȶ��ε�����Ϣȷ������ļ�������ʧ���ʡ���������ת¼�ʡ����ϳ����뽵���ʵȲ������������ɽ������mRNA�����뵰�ϳɵ��ַ����飬����ȷ��ÿ���������Ľṹ�������ַ��̱�ʾʽ���ǽ�ģ�о��Ĺؼ����⡣
����ʵ������ѵ��������ϸ���ر�̵�micro-array���ݡ������ó���������ʵ�����ݡ�ת¼������Ŀ����������ӽ��ǿ�ȵ�Chip-chip���ݵȵ�ʵ�����ݡ�����ԭλ�ӽ������뵥ϸ�����������Ȼ�õĵ�ϸ����̬�벿�ֻ�������ӫ����ɫ��õļ���ϵ��ص����ݡ�����ۺ�������Щ��ͬ���ʡ���ͬ��ʾ��ʽ��������������ʵ��������ݣ�ȷ������ֱ��������Զ�Ӧ��ϸ�����ͼ���ϸ������ת�����̵�ģ�Ͳ��������ǽ�ģ�Ĺؼ����⡣
���ڶ��������ַ��̵������ģ�ʹ����Ʋ���֮�临�ӵķ����Թ�ϵ�����������ַ�������Ļ������ģʽ��ʵ���������ƽ�����ۺ������ڶ���ֲ���С�㣬һ���Ż��㷨ֻ�ܻ�þֲ���С�㡣��λ��ȫ�����Ž����ԽϺõľֲ����Ž�Ҳ�ǽ�ģ�������ƵĹؼ����⡣
���⣬��������ʵ����������ɢʱ���IJ��������������ַ��̵�����������źţ���αȽ����ֲ�ͬʱ�����Ե����ݣ���ƺ����IJ��������Ż�����Ҳ��ģ�Ͳ������ƵĹؼ����⡣
c. ģ��ֲ�仯���ƵĹؼ�����
�ֲ�仯ģ�����Ҫ�����Ǿ����ֲ�IJ���������������Ч�ʹ��ͣ�������������м�״̬̫�࣬�������������ر�̹��̣������Ҫ����ÿ��·�������IJ���Ƿ�ƽ�У�ƽ�м����ܹ���ģ�͵��ǿ��ܻ���ʵ��ʵ��������ƫ�롣
3�����ȡ���о������������Է����������о�����������·�ߡ�ʵ���ֶΡ��ؼ�������˵������
���ȡ���о�����������·�ߣ�
����Ŀ��Ҫ�������ھ�ͼ��������Ϊ�����ۺ������źŴ�����ͳ���ƶ��Լ���Ϣ�۵��о���������ǰ�ؼ��������������о����������桢ʵ������ʵ��������ݽ�����֤���ϵ��о����������о�������ϵ�ǰ�������������о��������е��Լ���Ŀ���ѻ��۵�����о��ɹ���չ�������о���̽���������о�˼·��ͼ1��ʾ��������ɫ�����Ǹ���Ŀ���о��������ݡ�
1. ϸ���ر�̸��ιؼ������о�
���ݲ�ͬ����ϸ�������ر��ʱ���������ʵ�����ݣ��Աȳ���ϸ����iPSϸ���������ر���м�״̬ϸ������̥��ϸ���Ļ���������ݣ�Ѱ�Ҳ���������ͼ2Ϊ���ڶ�С�����άϸ��ʵ�����������������������
�ҵ����������ر��ʱ��ͬ�IJ���������ʹ��DAVID ( Database for Annotation, Visualization and Integrated Discovery) �Բ������������KEGG��Kyoto Encyclopedia of Genes and Genomes��ͨ·���������Է�����
����ת¼����������ĵ��ع�ϵ��Ѱ�ҹ�����ת¼���ӡ�ʹ��FastNCA�����㷨ȷ��һ���غ϶ȸߵ�ת¼���ӵĻ�Ծ�Ⱥ͵���Ӱ�졣����ʹ��STRING���ݿ�Ԥ�ⲻͬת¼���Ӽ�Ľ������ã�ͬʱʹ��FastNCA�����غ�ת¼�����Լ��ڲ�ͬ״̬ϸ������Щת¼���ӵİл���֮���ת¼����������
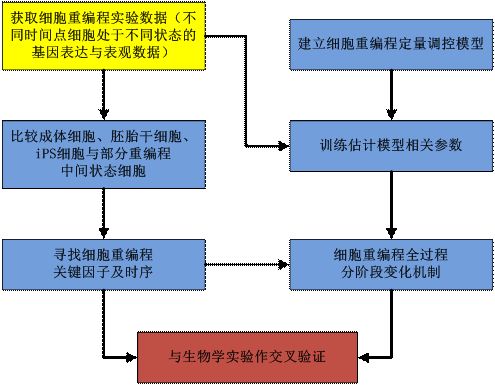
ͼ1 �����о�˼·
ͼ2 С�����άϸ���ر�̲���������
2. ϸ���ر�̶�������ģ�ͽ���
ϸ�����Ϳ�����ϵ�����ԵĹؼ�����ı���ģʽ��������һ������ı���ģʽ���������ת¼���ϳɣ��ͽ����ʾ��������ȷ��ϸ������ѡ���������Ĺؼ�����ȷ��ת¼�ͽ����ʣ���ת¼�뽵�����ܻ����Ե��ؼ���������Ļ����ء�
�Ե��������ڱ��ֻ���ı������������������ȱʧ�������Ҳ��ά���Լ��ı��������Ե��ر���Ϊ�����ڽ��Ͷ��ⲿ�����̼�����Ӧʱ�䣬�Ӷ����ӻ��������ȶ��ԣ�����ά��ϸ�����͵Ĺؼ������ػ�����Ե���һ����ͨ�����Լ��������ӽ�����γ����ĵ��ػ�·���̶��γ�����ӵ��Ե��ػ����ﵽ���ڱ�����������Ŀ�ġ������Ե������������ת¼�ʡ������������о�������ˮƽ����һ��ʵֵ�ķ����Ժ���ȷ�������ʵֵ�����Ժ���ͨ������Michaelis-Menten ��ϣ����ʽ����iPSϸ�������ڻ���Nanog ��Oct4Ϊ���� ���Ե��ض�ת¼�ʵĹ��ֱ�Ϊ��
Nanog: ʽ(1)
Oct4: ʽ(2)
����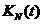 ��
��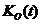 Ϊ���볣����
Ϊ���볣����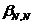 ��
��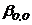 ���Ե���ת¼ǿ��
���Ե���ת¼ǿ��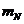 ��
��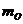 �ֱ�Ϊ�������ӵ�mRNAˮƽ��
�ֱ�Ϊ�������ӵ�mRNAˮƽ��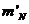 ��
��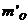 �ֱ��ǹ�ͬ����Nanog��Oct4�ϵ�ת¼���ӵĹ���Ӱ�죬�ⲿ�ֿɱ�����ת¼����ȡ�����ϱ�n��ϣ��������Эָͬ����һ��ȡn = 4��
�ֱ��ǹ�ͬ����Nanog��Oct4�ϵ�ת¼���ӵĹ���Ӱ�죬�ⲿ�ֿɱ�����ת¼����ȡ�����ϱ�n��ϣ��������Эָͬ����һ��ȡn = 4��
����Ҳ���Ե��������ı����Ŵ���Ⱦɫ��״̬������Ⱦɫ�ʽṹ������ת¼�����ӵĿɴ��Ժ�ת¼���ܵı��֣���˱����Ŵ�����ͨ���ı����ڰл����������ϵ�ת¼���ӵĽ��볣����Ӱ�����Ŀ��أ������볣���������Լ�mRNA ��ȵĺ�����
�����Ե��أ�����֮��Ļ����ض�ϸ������ѡ��Ҳʮ����Ҫ������ط������Ե��������Ƶ���ѧ��ʽ�����յĵ��ط��̽�����Ϊ�ַ��̵���ʽ��
ȷ����ģ�͵Ļ����ṹ���ַ��̣���һ���������ȷ������ģ���е����ɲ�����ģ����ÿ���������������͵����ɲ�������1���Ե��ء������غ��ⲿ�źŵ�ǿ�ȣ���2��������Ŵ�״̬��صĽ��볣���еIJ�������3���������еIJ�����
���ɲ���ȷ��ʹ��ƽ�������С��ԭ����ʹ���κ��Ż�������Ѱ��ʹƽ�������С�IJ�������ͳ�ķ��������ݶ�����������Ҫ�������δ֪������ƽ�������ݶȡ����������ַ��̽���м�����Щ�����Dz����ġ����⣬����ģ�͵ĸ����ԣ������ַ��̵Ľ����δ֪�����Ͳ�������ķ����Ժ�����Ŀ�꺯���ж���ֲ���С���Ҳ���ȫ�����Ž�Ľ�����ȣ����Dz��õĺ����Ż�������ֻ���ҵ�һ��Ŀ�꺯����һ���ֲ���Сֵ��Ϊ�������ҵ��õ���Сֵ�Ļ��ᣬ���������ڲ����Ż������У����ǽ���ʹ�������½������Ľ��ĵ����η����ֲ�ͬ�ļ�����Nelder-Mead �����η��ڲ����ռ��д�����һ�������Σ�������������ζ��㴦������ֵ��ÿ�������ʾһ�����ܵIJ�����ֵ��Ȼ��ͨ������������ߵ÷ֵĶ������������Σ�ֱ���ﵽһЩԤ����õı߽硣Ҫʹ�����ַ�����ֻ��Ҫ���㺯��������㣨�������ã���ֵ���ɣ��������ݶȡ����ڼ���չ��ʽ�������½���ͨ��������ϼ��������Եõ���ɢѵ�����ݵ��������������ƽ�������ݶȻ������½����¿���ͨ��һ�����ɲ��������㡣��ˣ��������ƿ������������½������档
3. ϸ���ر�̷ֲ�仯����ģ��
��ϸ���ر�̹����У�ϸ����ϵ��ά�ֺ�ת������һϵ�����ع�ͬ������ɵģ�������Ҫ����Ⱦɫ�ʵ����Ρ�ת¼���ӵ����ء��ڳ����ļ�ģ������Ҫ�����¼��裺
����1��ֻ���ǹؼ�����ı��������������
����2����ÿһ��ϵ�Ĺؼ�������Ϊһ�������ģ�鿼�ǡ�����ϵ�ؼ�������ܲ�ֹһ���������йؼ�������Ϊ���忼�ǣ�
����3����Ϊ��ͬ��ϵ�Ĺؼ�������ͬ��ʵ�ʲ�ͬ��ϵ�Ĺؼ���������в����غϣ�����������ϵ�Ĺؼ���������Ժܸߣ����ڽ�������Ϊ���忼��ʱ����Ϊ������ϵ�Ĺؼ����������
����4�������������ķֲ�ģ����������Ϊϸ���ķֻ����ر��������ij���ֲ��·�߷�չ�ģ���ʧһ���ԣ�������Ϊÿ���ڵ�ֻ��������֧��ϸ���仯����һ����ϵ��֧����������������ϵ������һ����֧��״̬��ת���ɹؼ�����ı���ͱ���״̬�ĸı����綨��
����5����ϸ�����ڼֳ����Σ���һ�μ��ں͵ڶ��η����ڡ��ڵ�һ�μ��ڣ�����״̬�����ģ������ڱ���״̬�������±���ڵڶ��η����ڣ����ݵ�һ�λ�������������Ļ���������״̬���ܷ����ı䡣
ģ���б���״̬��Ϊ������ۺͳ�Ĭ����״̬���ؼ�����������Ϊת¼�����ת¼��Ĭ����״̬�������ڵ�ʵ�������ؼ����������ڱ��۵�Ӱ����ѭ���¹���
����1�������ڽ������־���ڱ���ϸ��������ϵ�Ĺؼ�����ģ���ϣ���ά��ϸ����ϵ���ȶ���
����2�������ڽ���Ĭ��־���ڵ�����������Ȼ��ֵܵĹؼ�����ģ���ϣ�����ֹ������ϵ��ת���Լ�żȻ���ֵ��ر�̹��̣�
����3�������ڽ����۱�־���ڵ���ֱϵ����Ĺؼ�����ģ���ϣ���ʹϸ���ܹ���һ���ֻ���
����4�������ڰѴ���ͬһ��ϵ�ṹ���������ڽ��ľ�����ϵ��������ϵ�ĵ���ģ�鶼ͨ��DNA������Ĭ������ֹ������ϵ��ת���Լ�żȻ���ֵ��ر�̹��̡�
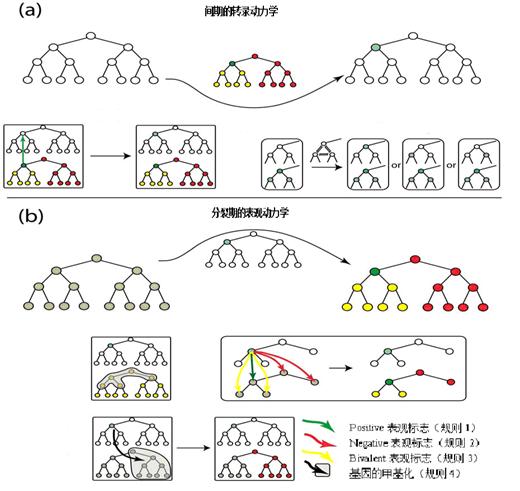
ͼ3 ����������������ù���
ǰ����������Ϊ�ɻ�����Ƶı���ֻ��Ӱ�쵽�������ֱϵ���ȡ�ֱϵ����������漰�����ȷֻ���������ֵܣ��Ļ���ģ���е��鵰�ױ�־������һ�ֽ�����ĵ��ع�����Զ����ĵ��ع�����ʱû��ʵ�������Եõ�ֱ�ӵĹ���������������ἰ�Էֻ�����������ϵDNA�����Ĺ۲��Լ�ȫ������ˮƽDNA�������谭ϸ���ֻ�������Щʵ���������ǿ������ݳ����ڻ��������ڷ����ڱ����ĵ�һ��Զ�̵��ع��������ĵĹ���4��
����״̬ȷ����������ļ��ڻ�����������ڱ���״̬���ڴ�ģ���б��۶Ի�������Ӱ������ѭ�Ĺ�����Ҫ�����㣺
����5�����м����־���������ڱ����Ϊ����״̬�������ڱ�����ǶԱ�������Ʋ���ӵ�г�Ĭ��־��DNA������ôǿ��
����6����������е�ʵ�����������ܵ��������ص�Ӱ�죬������ϵ�Ļ������ͬʱ�ܵ����ơ�
�ɼ����ʵ�������õĹ�����ģ�ͺɽ�ģ����������ǰ����ʵ������֤ģ�͵Ŀɿ��ԡ�
ʵ�鷽����ؼ�������
����Ŀ��Χ������ѧʵ�顢ʵ�����ݺ�����������Դ��չ�о��ģ��������ʵ�鼰ʵ������ʮ����Ҫ���о��н����ý�����������о������ģ����֤���������ݿ��������ϵķ���������֤��
ϸ���ر�̸��θ���ϵϸ���Ļ��������������ݿɴ�������Ϳ�Դ���ݿ��л�ȡ����������ģ�ͺ�ģ��ֲ�仯��������Ҫ���ʵ�����ݽ���ģ�Ͳ���ȷ����ģ����֤���ο����װ����˾���������Դ��
�����Է�����
ǰ��������о�����������·�������У������о�����������������ǰ�����㡢��ʵ�������˲��ּ�������棬�Ը��ֿ��ܵ���������꾡��������档Ԥ���ڽ�һ�������о��Ļ����ϣ��ɻ������Ľ��ۡ�
����Ŀ�о������ǽ���������о��ȵ㣬�д������ʵ�����ݣ�ͬʱ����������Դ���ݿ�������ݻ�ȡҲ�����㣬��Ŀ�о�����Ҫ��������Դ�ḻ���μ�ʵ�鷽�����֣����ӹ������о���״���п�֪�������������չ�˴��������Ŀ������ص��о�����ȻȺ��ϸ��ƽ����ѧģ���о���ϸ���ر�̵Ľ��о���������ȱ�������⣬��ϸ��ˮƽ�ĵ���ģ�����ر�̵Ľ����о��в����죬��ȴ�ṩ��һ���Ӷ����Ƕȷֽ��о�ϸ���ر�̵���Ч;������������Ŀ���о������ǿ��еġ�
��Ŀ�����˽�����һֱ����������Ϣ������ͳ���źŴ����ȷ�����о�����iPS�γɻ��ơ�ϸ���ر�̽�ģ��ؼ����Ӳ��ҵȷ��淢���˶�ƪSCI���ģ��μ��о�������������֣���Ϊ����Ŀ�о����������õ����ۻ�����
��Ŀ�Ŷ������Ա�긻��ǿ������ḻ����ɺ�������Ա�Ⱦ��зḻ���źŴ����������ָ������������������Ƶ�����ѧ��ģ�������ģ��ȷ�����Է���������ͬʱ���Ŷ�����ʵ����ӵ�зḻ���о�����Դ�����Գе����ģ����湤����
����Ŀ���е�λ��������ѧѧԺ��ҽѧԺ��ӵ�й���һ����ʵ�����豸�뼼����������Ҫ������Ϊ����Ŀ�о����ý��۽���ʵ����֤��
��ˣ��ۺϿ�����Ŀ���о����ۻ��������������Դ����Ա�豸��������Լ�ʵ����֤���������˵����Ŀ�ܹ�����Ԥ��Ŀ��˳����չ��
4������Ŀ����ɫ�봴��֮����
����Ŀ�ںϹ������ڶ�����ѧʵ��ɹ���ͨ���Ƚ��о�ϸ���ر�̻��ƣ�̽��Ӱ���ر��Ч�ʵ����ء��������ڶ����ϸ���ر�̵��о���ȣ�����Ŀ����ɫ�봴��֮����Ҫ�������ĵ㣺
1. ��Ȼϸ���ر����һ���������̣����е��о����Ҳ������Ϊһ�������о����������о��ɹ��Ѿ���ʾ������̿��Է�Ϊ�������ԵĽΣ�����Ŀ�������о�ϸ���ر�̵Ľ���ʱ��Ѱ��ÿ���εĹؼ��¼������ӣ�
2. ���ж���ϸ���ر�̵��о���ཫ�о������趨Ϊϸ��Ⱥ�壬�õ�����Ⱥ��ϸ����ͳ��ѧ���ɣ���ʵ����ֻ�в���ϸ���ܹ��ɹ������ر�̣����ڵ�ϸ�����о�������ʵ�����塣����Ŀ����������������������ɢʱ��������ѧ���飬������ϸ��ˮƽ�ϵ�ϸ����̵���ģ�ͣ�
3. �����о�����ϸ���ر�̹��̴���ȷ��������������ֶ����۵㣬��Ŀǰ���о�֧�����ֹ۵��ʵ��۲������г��֡���ˣ�����Ŀ�ڽ���ģ��ʱ��ͻ����ǰ�о��ж�����ȷ����ģ�ͺ����ģ�;����ԣ����������ȷ��������������ϵ�ģ������iPS�����Ĺ��̣���ÿ���������ӵļ���������¼�����һϵ�����Ӽ�����ȷ����ʱ������ʵ��ʵ���������Ǻϵģ�
4. ����Ŀ�о��ۺϿ��Ƕ��εĵ������أ��������������ϸ������״̬�����������֯�ĵ�������ģ�ͣ��Ƕ�Ŀǰ�ڶ�����о�ij��Ӱ�����ص�һ�ִ��¡�
5������о��ƻ���Ԥ���о��������������֯����Ҫѧ������������ʺ����뽻���ƻ��ȣ���
����о��ƻ�:
����Ŀ��������ʱ����ɸ����о�������ƻ��������£�
2018.01~2018.08 �ռ���������ʵ��ɹ����Աȷ�����ϸ���������ر��ϸ����iPSϸ������̥��ϸ���ı�����������ݣ�Ѱ�Ҳ���������ȷ���ر�̹��̸��ιؼ�����ģ�顣
2018.09~2019.09 ϸ���ر�̶�������ģ���о������ɰ���ת¼�����Ե����뻥���ء�Ⱦɫ�忪��״̬����ϵ����֮��ĶԿ����ⲿ�źŷ���ͨ·��ϸ���������ڽṹ�ȶ�������Ϣ��������ϸ���Ķ��������ַ��̣�����ģ�ͽṹȷ�����������ƽ�ģ�ȡ��ڼ�μ�һ��ѧ�����齻����
2019.10~2020.10 ϸ���ر�̵ķֽ��о��������ر�̹����йؼ�����ı��������״̬�����б�Ҫ�����ļ��裬����ϸ���ر�̵Ķ������ֲ�ģ�ͣ��о��ر�̹�����ϸ���ػص�����̬��·�����о���ֲ�仯���ơ��ڼ�μ�һ��ѧ�����齻����
2020.11~2020.12 ���ɣ������������ܽᲢ�ύ�о��������ܽᱨ�档
Ԥ���о����:
ȷ��ϸ���ر�̸��εĹؼ����Ӽ�ʱ��ڵ㣬���ɰ�������ת¼�����Ե����뻥���ء���ػ���Ⱦɫ�忪��״̬������ϵϸ���ؼ�����֮��ĶԿ����ⲿ�źŷ��Ӽ�����ϸ���������ڽṹ�ȶ��ε�����Ϣ������ϸ���ر����صĹؼ�����Ķ�������ģ�ͣ��ڴ˻������о�̽��ϸ���ر�̵ķֽα仯���ƣ�ģ����仯���̣���ȡʵ���о�����õĶ������ػ�����Ϊ���ϸ���ر��Ч����ɿ��Ե��ṩ����ָ������ѧ����ģ�͡�
����Ŀ��Ϊ�����о����������ۼ�ʵ���о����������ʽ���������ġ�ѧ��������ʽ������Ԥ�ƽ���ɹ����ڿ�����1-2ƪ������Ȩ����������1-2ƪ����������2ƪ��ͨ������Ŀ���о������������о�ˮƽ��ȡ����ﵽ�����Ƚ�ˮƽ����ȡ��ýϴ����Ч�档
�ڱ���Ŀ�����£�����������3��˶ʿ�о���, 10 ��������(��ҵ���)��
�������о������빤������
1���о��������뱾��Ŀ��ص��о��������ۺ���ȡ�õ��о������ɼ�����
�����˳��ڴ���������Ϣ�������źŴ����������ھ����������о����������õ����ۻ�����������ʿѧλ�ڼ䣬�ڵ�ʦָ���²����˶��������Ȼ��ѧ������Ŀ�о���˶ʿ��Ҳ��������漰�źŴ����ľ�����Ŀ������������ѧ���ڿ������ѧ�������Ϸ�������ʮ��ƪ������SCI�ڿ�������ƪ����һ������ƪ������ƪSCI/EI�������ļ����ں����ڿ����ģ��μ��ɹ��б�����
Ŀǰ����������ȡ�õ��뱾��Ŀ��ص���Ҫ�о��ɹ��У�
��1�� ��ϸ���ر�̹ؼ�������iPS���������о�
ͨ���ռ���Դ���ݿ��д����й�iPSϸ����ʵ�����ݣ�ʹ�������ھ�ȷ�����������Ϣ�����ںϷ����������ϸ������̥��ϸ���Ƚϣ�Ѱ�ҳɹ�ʵ����ϸ���ر�̵Ĺؼ����ӣ�̽����ϸ���ر�̻��ƣ�����Ϊ��Ч��ð�ȫ��iPSϸ��ʵ���ṩ�������ݡ�������������IJμ��ɹ��б�[1][8][10][11]��
��2�� ������������״̬��ϸ����ϵѡ���Ӱ��
�����˺���ϸ����ͬ��ϵ�Ļ���������ݣ�ȷ����ͬ��ϵϸ���IJ����������ݲ���������Ĺ��ܼ����ź�ͨ·������������ϵ�������������硢���ת¼���ӽ�������̽����ϵת����������ϵ�ؼ�����ļ����Ĭ����Ҫ�¼�����ϸ����ϵѡ���Ӱ�졣ͬʱ���ɺ�С�嶨λ���ݼ��㣬Ѱ�Ҿ�����С�嶨λ��Ӱ�����أ����ڻ�ú�С�嶨λ�ȱ����������������ϸ�������ԵĹ�ϵ����һ������о���Ҫ����˹�����Ȼ��ѧ���������ѧ������Ŀ���ں�DNA��ά�ṹ��Ϣ�����ת¼�����о�����������������IJμ��ɹ��б�[2][6][7][9]��
��3�� ϸ����ϵѡ��ģ
���ݴ��������е�����ʵ������������ת¼���ӡ��������Ρ�ϸ���������ڡ���ϵ�������ӶԿ������أ�������ϸ��ͳ��ģ�ͣ�������̽����ϸ���ر���ж���Ӱ����Ч�ʵ����ء���һ������о���Ҫ����˹�����Ȼ��ѧ������Ŀ��ϸ�����˿���ͳ��ģ�ͽ�ģ�������������������������IJμ��ɹ��б�[3][5]��
��4�� �������븴��ϵͳ����
��������˶ʿ����Ҫ���кϳɿ��״����ݴ������߱��ḻ�Ĵ����ݴ���ʵ�ʾ��飬������������IJμ��ɹ��б�[4][12][13]��
2�����������������Ѿ߱���ʵ����������ȱ�ٵ�ʵ��������������;�����������ù���ʵ���ҡ������ص�ʵ���ҺͲ����ص�ʵ���ҵ��о����صļƻ�����ʵ�������
�������������뵥λӵ��ϵͳ����ʵ����Ӳ��ƽ̨�������㶫ʡ������Ϣ����ʵ���ѧʾ�����ģ��㶫ʡ���������ʵ���ѧʾ�����ģ��㶫ʡ�������ִ����Ӽ����ص�ʵ���ҵȣ��������õ�ʵ���豸�������о��Ŷ���Ա�긻��ǿ����ɺ����������зḻ�������ھ��źŴ������鼰��Ӧ����Ŀ���������ܱ�֤�ڸڿ���ʱ�䡣����ʵ���ҳ����������������о�������Э�������Ŀ�ı�̷�������
ͬʱ���������Բ�ʿ�ڼ�����һֱ���䲩ʿ������λ��ɽ��ѧ%%����ʵ���ұ������н�����������ʵ������������Ϣ���������ڹ���֪����������ˮƽ����������α�����Ȩ���ڿ���¼������һƪ��Ϊ�ڿ���������ߵ�ʮƪ����֮һ���������Ϲ��ʶ���ѧ���������ļ����档����ĿҲ���Ӹ�ʵ���һ�ü���ָ����֧�֡�
Ŀǰ�������Ŷ�������ȱ�ٵ�ʵ������Ϊ����ʵ���������������������е����뵥λӵ�й���֪���ĸ���ҽԺ��������ѧѧԺ�������˿ɻ������Ҫ��ʵ�����ݣ��Ҹ���Ŀ�����������֤ʵ���Ϊ��ͨʵ�飬�κξ߱���Ӧ�豸����Ա������ʵ���Ҿ����Գе���
3�����ڳе����뱾��Ŀ��صĿ�����Ŀ����������˺���Ŀ����Ҫ���������ڳе����뱾��Ŀ��صĿ�����Ŀ���������������Ȼ��ѧ�������Ŀ���������Ƽ��ƻ���Ŀ��Ҫע����Ŀ�����ƺͱ�š�������Դ����ֹ���¡��뱾��Ŀ�Ĺ�ϵ����������ݵȣ���
1. ������Ȼ��ѧ����������Ŀ��61174163��ϸ�����˿���ͳ��ģ�ͽ�ģ�����������2012/01-2015/12��63��Ԫ���ѽ��⣬�μӣ�
2. ������Ȼ��ѧ���������ѧ������Ŀ��61202343���ں�DNA��ά�ṹ��Ϣ�����ת¼�����о���2013/01-2015/12��28��Ԫ���ѽ��⣬�μӡ�
4����ɹ�����Ȼ��ѧ������Ŀ������������˸����ǰһ���ѽ����ѧ������Ŀ����Ŀ���Ƽ����ţ��������������о���չ���뱾������Ŀ�Ĺ�ϵ������ϸ˵�����������ѽ�����Ŀ�о������ܽ�ժҪ����500�֣�����سɹ�����ϸĿ¼����
��
������������Ҫ˵��������
1. ������ͬ�����벻ͬ���͵Ĺ�����Ȼ��ѧ������Ŀ���������ͬ�������������Ŀ����Ŀ���͡���Ŀ������Ϣ����˵���뱾��Ŀ֮�����������ϵ����
��
2. ���и�רҵ����ְ��ְ�ƣ��������˻�����Ҫ�������Ƿ����ͬ��������߲������������Ȼ��ѧ������Ŀ�ĵ�λ��һ�µ���������������������������漰��Ա���������������������������Ŀ����Ŀ���͡���Ŀ���ơ���λ���ơ�������Ա�ڸ���Ŀ���������˻��Dz����ߣ���˵����λ��һ��ԭ��
��
3. ���и�רҵ����ְ��ְ�ƣ��������˻�����Ҫ�������Ƿ���������ڳе��Ĺ�����Ȼ��ѧ������Ŀ�ĵ�λ��һ�µ���������������������������漰��Ա�����������ڳе���Ŀ�����š���Ŀ���͡���Ŀ���ơ���λ���ơ���ֹ���£���˵����λ��һ��ԭ��
��
4. ������
��

