
杨更光 河南省郑州市第七人民医院普外科 450047
徐世国 浙江大学附属第一医院普外科 310006
摘要 目的 探讨替吉奥辅助化疗对行胰头十二指肠切除术的老年胰腺癌患者术后免疫功能及预后的影响。方法 选取2013年2月-2014年7月本院收治的老年胰腺癌患者79例,均行胰头十二指肠切除术治疗,将患者随机分为对照组(n=39)及观察组(n=40),对照组患者采用吉西他滨辅助化疗,观察组患者在对照组的基础上联合替吉奥辅助化疗。检测化疗前后2组肿瘤标志分子水平、免疫球蛋白含量、T淋巴细胞亚群及NK细胞比例;统计2组近远期临床疗效及治疗期间不良反应。结果 与化疗前比较,化疗后2组血清CA19-9、CA50、CA125及CA242水平明显降低(P<0.01),且观察组显著低于对照组(P<0.05或P<0.01);与化疗前比较,化疗后2组血浆IgG、IgA及IgM含量均明显升高,且观察组显著高于对照组(P<0.05或P<0.01);与化疗前比较,化疗后2组CD4+、CD8+比例及NK细胞比例均显著降低,但观察组CD4+比例及NK细胞比例显著高于对照组,CD8+比例显著低于对照组(P<0.05或P<0.01);化疗前后对照组CD4+/CD8+比值无显著变化,而观察组化疗后CD4+/CD8+比值明显增加,且显著高于对照组(P<0.01)。观察组总有效率为82.50%,显著高于对照组的58.97%(P<0.05),且观察组术后1年、2年生存率也显著高于对照组(P<0.01)。2组均无严重不良反应。结论 替吉奥辅助化疗可显著降低行胰头十二指肠切除术的老年胰腺癌患者术后血清肿瘤标志分子水平,保护其免疫功能,提高患者临床疗效及远期生存率,并具有一定的安全性。
关键词 胰腺癌; 胰头十二指肠切除术; 替吉奥; 吉西他滨; 免疫; 预后
胰腺癌是一种恶性程度较高的消化系统恶性肿瘤疾病,其病程短、病情进展迅速,且发病率逐年升高。严重威胁人们生命健康[1-2]。胰腺癌患者早期便表现出局部浸润,甚至远处转移,其发病隐匿,确诊难度大,就诊时大多已进展至中晚期,死亡率较高。胰头十二指肠切除术是胰腺癌根治的唯一方法,但其治愈率较低,预后较差。目前,术后辅助化疗已成为延长胰腺癌患者生存期和提高生存率的关键[3]。替吉奥是一种生物利用度较高的抗癌药物,据报道[4],术后替吉奥辅助化疗可显著改善胰腺癌手术患者的预后。本研究旨在探讨替吉奥辅助化疗对行胰头十二指肠切除术的老年胰腺癌患者术后免疫及预后的影响,现报道如下。
1 资料与方法
1.1 一般资料 选取2013年2月-2014年7月本院收治的胰腺癌患者79例,所有患者均经临床病理检查确诊且行胰头十二指肠切除术治疗。纳入标准:年龄>65岁;无胰头十二指肠切除术禁忌证;病灶直径2-5 cm;无放疗或化疗史者。排除标准:血常规检测异常者;合并严重心、肝、肾等重要脏器疾病者等。所有纳入患者及家属均签署知情同意书,且本研究经本院医学伦理委员会研究批准。
将患者随机分为对照组(n=39)及观察组(n=40),对照组男20例,女19例;年龄66-78岁,平均(71.3±9.6)岁;疾病类型:腺泡细胞癌7例,导管腺癌32例;TNM分期:Ⅰ期11例,Ⅱ期20例,Ⅲ期8例。观察组男20例,女20例;年龄67-79岁,平均(70.9±9.3)岁;疾病类型:腺泡细胞癌9例,导管腺癌31例;TNM分期:Ⅰ期13例,Ⅱ期21例,Ⅲ期6例。2组主要一般资料比较无显著性差异(P>0.05),组间具有可比性。
1.2 方法 2组均行胰头十二指肠切除术治疗,术后第6周对照组行辅助化疗:采用注射用吉西他滨(海南锦瑞制药有限公司,国药准字H20163172,0.2 g)化疗,1 000 mg/m2与250 mL的氯化钠注射液混合,静脉滴注,1次/周,连续治疗6周。观察组在对照组的基础上采用替吉奥胶囊(山东新时代药业有限公司,国药准字:H20080802,20 mg/粒)辅助化疗:口服40-60 mg,早晚各服1次,连续服用2周后停药1周,3周为1个周期,2组均连续化疗2个周期。
1.3 观察指标 (1)分别采集2组患者化疗前后空腹静脉血5 mL,经离心分离血清,采用生物芯片检测仪检测2组血清CA19-9、CA50、CA125及CA242等肿瘤标志物水平;(2)采用ELISA法检测2组血浆免疫球蛋白含量(IgG、IgM及IgA等);采用流式细胞术检测2组全血中CD4+、CD8+等T淋巴细胞亚群及NK细胞比例,计算CD4+/CD8+;(3)统计2组临床疗效:完全缓解:病灶消失,且维持至少4周;部分缓解:病灶面积缩小至少30%,且持续超4周以上;稳定:病灶面积缩小<30%,或有所增大;进展:病灶面积增大20%以上,或发现新病灶。临床总有效率=(完全缓解例数+部分缓解例数+稳定例数)/总例数×100%。术后定期随访2年,统计2组患者远期生存率,包括术后半年、1年及2年生存率;(4)统计2组患者治疗期间不良反应。
1.4 统计学方法 采用SPSS 19.0软件对数据进行统计学分析,计量资料以均数±标准差(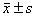 )表示,多组间计量资料比较采用重复测量方差分析,2组间比较采用t检验;计数资料以百分比(%)表示,采用χ2检验。以P<0.05为差异有统计学意义。
)表示,多组间计量资料比较采用重复测量方差分析,2组间比较采用t检验;计数资料以百分比(%)表示,采用χ2检验。以P<0.05为差异有统计学意义。
2 结果
2.1 化疗前后2组血清肿瘤标志物水平比较 化疗前2组肿瘤标志物水平无显著性差异(P>0.05);与化疗前比较,化疗后2组血清CA19-9、CA50、CA125及CA242水平明显降低(P<0.01),且观察组显著低于对照组(P<0.05或P<0.01)。见表1。
表1 化疗前后2组血清肿瘤标志物水平比较(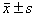 ) U/mL
) U/mL
|
指标 |
对照组(n=39) |
观察组(n=40) |
|
化疗前 |
化疗后 |
化疗前 |
化疗后 |
|
CA19-9 |
306.6±52.5 |
275.3±41.5** |
307.1±53.2 |
255.6±38.3**# |
|
CA50 |
77.8±8.4 |
59.2±6.4** |
78.1±8.3 |
54.6±5.3**## |
|
CA125 |
62.3±7.5 |
43.8±5.4** |
61.9±7.4 |
38.6±5.2**## |
|
CA242 |
41.1±5.2 |
28.5±3.3** |
41.0±5.3 |
24.3±2.9**## |
与化疗前比较,**P<0.01;与对照组比较,#P<0.05,##P<0.01。
2.2 化疗前后2组患者免疫功能比较
2.2.1 化疗前后2组血浆免疫球蛋白含量比较 化疗前2组血浆免疫球蛋白含量无显著性差异(P>0.05);与化疗前比较,化疗后2组血浆IgG、IgA及IgM含量均明显升高,且观察组显著高于对照组(P<0.05或P<0.01)。见表2。
表2 化疗前后2组血浆免疫球蛋白含量比较(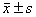 ) g/L
) g/L
|
指标 |
对照组(n=39) |
观察组(n=40) |
|
化疗前 |
化疗后 |
化疗前 |
化疗后 |
|
IgG |
12.5±2.3 |
14.6±2.4** |
12.4±2.4 |
17.4±2.3**## |
|
IgA |
2.2±0.5 |
2.6±0.5** |
2.2±0.4 |
3.0±0.6**## |
|
IgM |
0.9±0.2 |
1.2±0.3* |
0.9±0.1 |
1.5±0.2**# |
与化疗前比较,*P<0.05,**P<0.01;与对照组比较,#P<0.05,##P<0.01。
2.2.2 化疗前后2组T淋巴细胞亚群及NK细胞比例比较 化疗前2组T淋巴细胞亚群比例、NK细胞比例均无显著性差异(P>0.05);与化疗前比较,化疗后2组CD4+、CD8+比例及NK细胞比例均显著降低,但观察组CD4+比例及NK细胞比例显著高于对照组,CD8+比例显著低于对照组(P<0.05或P<0.01);化疗前后对照组CD4+/CD8+比值无显著变化,而观察组化疗后CD4+/CD8+比值明显增加,且显著高于对照组(P<0.01)。见表3。
表3 化疗前后2组T淋巴细胞亚群及NK细胞比例比较(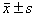 )
)
|
指标 |
对照组(n=39) |
观察组(n=40) |
|
化疗前 |
化疗后 |
化疗前 |
化疗后 |
|
CD4+/% |
36.4±5.3 |
32.3±6.2** |
36.8±6.1 |
33.6±5.1**# |
|
CD8+/% |
37.7±3.8 |
32.2±4.0* |
37.1±2.8 |
28.2±3.9**## |
|
CD4+/CD8+ |
0.9±0.2 |
1.0±0.3 |
0.9±0.2 |
1.5±0.3**## |
|
NK细胞/% |
9.2±1.3 |
6.2±0.9* |
9.6±1.1 |
8.1±1.1**## |
与化疗前比较,*P<0.05,**P<0.01;与对照组比较,#P<0.05,##P<0.01。
2.3 2组近远期临床疗效比较
2.3.1 化疗后2组临床有效率比较 化疗后观察组完全缓解3例,部分缓解17例,稳定13例,进展7例;对照组完全缓解1例,部分缓解7例,稳定15例,进展16例。观察组总有效率为82.50%(33/40)显著高于对照组的58.97%(23/39)(P<0.05)。
2.3.2 2组远期生存率比较 对照组半年生存率89.74%(35/39),1年生存率43.59%(17/39),2年生存率33.33%(13/39);观察组半年生存率92.50%(37/40),1年生存率77.50%(31/40),2年生存率67.50%(27/40);与对照组比较,观察组术后1年、2年生存率显著升高(P<0.01)。
2.4 不良反应 2组间均未见严重不良反应,主要不良反应包括皮疹、乏力、厌食、恶心、腹泻或口腔黏膜炎等,经对症治疗均逐渐缓解。
3 讨论
胰腺癌发病迅速,可在短期内发生远处转移,造成极其严重的并发症,严重危害人类健康。手术切除是根治、延长胰腺癌患者生存率的有效途径,胰头十二指肠切除术是其经典术式,但患者术后复发率高、生存率低、预后较差。因此术后常需结合辅助化疗等方式以期提高患者术后生存质量[5]。吉西他滨属于二氟核苷类药物,是较为常用的抗癌药物,可阻碍肿瘤细胞DNA复制,促进其凋亡、坏死[6-7]。替吉奥胶囊主要是由替加氟、奥替拉西、吉美嘧啶等复合而成,具有较高的生物利用度,可选择性拮抗消化道内分布的乳清酸磷酸核糖基转移酶,经肝药酶反应转化为5-氟尿嘧啶(5-Fu),从而达到抗癌功效[8]。两者均可用于肿瘤患者术后辅助化疗,但有关两者在胰腺癌患者术后联合应用辅助化疗的研究尚鲜有报道。
胰腺癌患者肿瘤组织中CA19-9、CA50、CA125及CA242等肿瘤标志物水平显著高于癌旁组织及正常组织,其对肿瘤的诊治、预后评估具有重要参考价值。通常肿瘤切除术后患者血清肿瘤标志物水平会显著下降,本研究中化疗后2组血清CA19-9、CA50、CA125及CA242水平明显降低,且观察组显著低于对照组,与周志鹏等[9]研究报道相似。提示替吉奥辅助化疗可有效降低老年胰腺癌患者术后肿瘤标志分子水平,较常规化疗药物吉西他滨的抗肿瘤效果更为显著,可能是由于其中的吉美嘧啶可有效阻止5-Fu分解,延长5-Fu在肿瘤组织、血液中的起效时间,增强替吉奥的抗癌作用。老年胰腺癌患者本身机体机能减退,加上术中创伤致使其表现为一定程度的免疫功能障碍。由B淋巴细胞分泌产生的免疫球蛋白是介导机体体液免疫应答主要效应因子,其与抗原结合形成复合物,进而抑制病原菌对机体的损害。本研究中化疗后2组血浆IgG、IgA及IgM含量均明显升高,且观察组升高更为明显;化疗后2组CD4+、CD8+比例及NK细胞比例均显著降低,但观察组CD4+比例及NK细胞比例显著高于对照组,CD8+比例显著低于对照组;化疗前后对照组CD4+/CD8+比值无显著变化,而观察组化疗后CD4+/CD8+比值明显增加,且显著高于对照组,与国内外研究报道[10-11]一致。提示吉西他滨联合替吉奥胶囊可提高患者术后体液免疫功能,且对患者细胞免疫功能影响较轻,有助于调节机体的免疫功能,恢复患者免疫力。此外,本研究中观察组总有效率为82.50%,显著高于对照组的58.97%,观察组1年、2年生存率也较对照组显著提高,同时2组不良反应均较轻微。提示吉西他滨联合替吉奥胶囊可提高老年胰腺癌患者术后临床疗效及远期生存率,且不增加老年胰腺癌患者术后并发症,具有较高的安全性,可能是由于替吉奥胶囊中奥替拉西在胃肠组织中具有较高的浓度,减少胃肠组织中5-Fu的分布,进而抑制胃肠道等不良反应的发生,与陈菊香等[12]报道相似。
综上,在常规化疗的基础上联合替吉奥辅助化疗,可明显降低老年胰腺癌患者术后血清肿瘤标志分子,促进患者术后免疫功能的恢复,明显提高临床疗效及远期生存率,且具有较高的安全性,预后良好,有望成为胰腺癌患者切除术后辅助化疗的标准方案。
参考文献
[1] 陈东升, 吴光兴, 唐丽珠. 胰腺癌根治术后行吉西他滨联合替吉奥化疗的临床观察[J]. 实用癌症杂志, 2014, 29(1): 78-80.
[2] Apte MV, Park S, Phillips PA, et al. Desmoplastic Reaction in Pancreatic Cancer: Role of Pancreatic Stellate Cells[J]. Cancer Letters, 2015, 29(3): 179-187.
[3] 李洪波, 刘崇忠. 胰头十二指肠切除术联合替吉奥治疗胰腺癌的临床观察[J]. 中国普通外科杂志, 2015, 24(9): 1232-1236.
[4] Nakai Y, Isayama H, Sasaki T, et al. A multicenter randomized controlled trial of gemcitabine (G) alone versus gem-citabine and S-1 combination therapy (GS) in patients with unresectable advanced pancreatic cancer (PC): GEMSAP study[J]. J Clin Oncol, 2010, 28(15 Suppl): 4037.
[5] 柯丽红, 罗会芹, 胡小秀, 等. 吉西他滨联合替吉奥对比联合奥沙利铂一线治疗晚期胰腺癌的临床疗效分析[J]. 肿瘤药学, 2014, 4(6): 441-445.
[6] Greenhalf W, Ghaneh P, Neoptolemos J P, et al. Pancreatic cancer hENT1 expression and survival from gemcitabine in patients from the ESPAC-3 trial[J]. JNCI: Journal of the National Cancer Institute, 2014, 106(1): 4796-4804.
[7] 陈光新. 吉西他滨联合顺铂对晚期胰腺癌的疗效分析[J]. 中国现代普通外科进展, 2015, 18(9): 730-732.
[8] 赵增虎, 王明贤, 尚培中, 等. 吉西他滨联合替吉奥方案化疗同步调强放疗治疗胰腺癌42例临床观察[J]. 山西医药杂志, 2014, 43(14): 1695-1697.
[9] 周志鹏, 谭向龙, 王维君, 等. 胰头十二指肠切除术后替吉奥辅助化疗对老年胰腺癌患者预后及免疫功能影响分析[J]. 中国医学前沿杂志电子版, 2016, 8(6): 172-175.
[10] 王欢. 吉西他滨联合替吉奥胶囊化疗对胰腺癌根治术后患者生存质量的影响[J]. 中华高血压杂志, 2014, 22(1): 13-14.
[11] Gürlevik E, Fleischmann-Mundt B, Brooks J, et al. Administration of Gemcitabine after Pancreatic Tumor Resection in Mice Induces an Anti-tumor Immune Response Mediated by Natural Killer Cells[J]. Gastroenterology, 2016, 151(2): 338-350.
[12] 陈菊香, 周红轩, 马兰, 等. 吉西他滨联合奥沙利铂或替吉奥对比吉西他滨单药治疗晚期胰腺癌临床观察[J]. 安徽医药, 2015, 19(2): 359-362.

